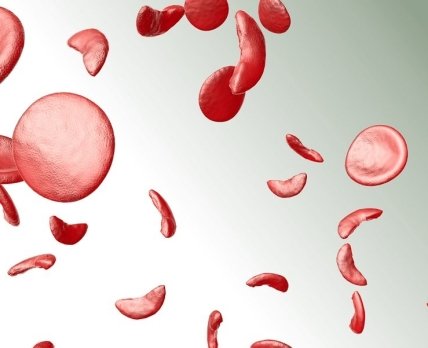
Дорогий препарат стане доступним для пацієнтів із серповидно-клітинною анемією у Великій Британії відповідно до позитивних рекомендацій, виданих Національним інститутом охорони здоровʼя та клінічного вдосконалення (NICE).
Нещодавно NICE оприлюднив остаточний проект настанови, що рекомендує Національній службі охорони здоровʼя (NHS) Англії покривати витрати на Casgevy для відповідних пацієнтів. Право на таке лікування матимуть пацієнти віком від 12 років з важкою серповидно-клітинною анемією, рецидивуючими вазооклюзійними кризами та певним генотипом.
Casgevy (ексагамглоген аутотемсел) — препарат генотерапії для однократного застосування, який було спільно розроблено компаніями Vertex Pharmaceuticals і CRISPR Therapeutics для лікування серповидно-клітинної анемії та бета-таласемії. Обидва захворювання спричиняються мутаціями в гені бета-субодиниці гемоглобіну (бета-глобіну, HBB).
Агентство з регулювання лікарських засобів та охорони здоровʼя Великої Британії (MHRA) схвалило Casgevy для лікування серповидноклітинної анемії у 2023 році, а потім у січні 2024 року було його схвалено для лікування трансфузійно-залежної бета-таласемії). При цьому Національна служба охорони здоровʼя Англії досягла попередньої угоди про відшкодування витрат для Casgevy при бета-таласемії раніше, ніж при серповидно-клітинній анемії — у серпні 2024 року.
На відміну від трансплантації донорських стовбурових клітин – єдиного доступного на даний момент методу лікування серповидно-клітинної анемії – Casgevy не несе такого ж ризику розвитку реакції трансплантат проти господаря (РТПГ). Однак він рекомендований NICE лише для пацієнтів, які мають право на трансплантацію, але не мають відповідного донора. За оцінками NHS, у Великій Британії налічується приблизно 50 таких пацієнтів.